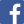- HUMAN Diagnostics Worldwide | Spanish
- Profesionales de laboratorios
- Tendencias y temas
Malaria: Pequeñas picaduras que amenazan al mundo
La salud pública está siendo amenazada por la propagación de las enfermedades transmitidas por vectores mientras que la falta de una solución diagnóstica adecuada para el tratamiento y la eliminación de estas enfermedades sigue siendo un desafío. Sin embargo, un nuevo método podría cambiar el panorama en la lucha contra la malaria.
Enfermedades transmitidas por vectores (VBD en inglés)
Recientemente ha habido mucho interés en la enfermedades transmitidas por vectores debido a la propagación del virus del Zika que podría causar el defecto de nacimiento de la microcefalia.
Las enfermedades transmitidas por vectores pueden ser fatales o causar debilitamiento en el paciente constituyendo más del 17% de las enfermedades infecciosas a nivel global. Cada año más de mil millones de personas se infectan y más de un millón mueren a causa de las enfermedades transmitidas por vectores1. Aunque las infecciones se dan principalmente en las regiones tropicales y subtropicales, el aumento de los viajes intercontinentales, la urbanización y el cambio climático contribuyen a que se presenten brotes en nuevas regiones. No solo en escenarios de recursos limitados prevalece todavía la falta de pruebas de diagnóstico rápidas, precisas y de costos razonables haciendo de las enfermedades transmitidas por vectores las más difíciles de prevenir y controlar dentro de las enfermedades infecciosas. Por lo tanto una de las principales formas de prevención es concienciar a las personas sobre la importancia de un diagnóstico preciso, hábitos de saneamiento y mecanismos adecuados de control de vectores. HUMAN está comprometida en la lucha contra las enfermedades infecciosas, especialmente en emplazamientos de recursos limitados. En una serie de artículos bajo el título Pequeñas picaduras que amenazan al mundo discutiremos las posibilidades de diagnóstico para ciertas enfermedades transmitidas por vectores.
Ejemplos de enfermedades transmitidas por vectores con el vector y patógeno respectivos
-
Enfermedad Vector Patógeno Malaria Mosquito hembra (género Anopheles) Parásito Plasmodium Dengue Mosquito hembra (Aedes aegypti) Virus del dengue Zika Mosquito de la especie Aedes Virus del Zika Chagas Insectos triatóminos Trypanosoma cruzi Tripanosomiasis africana Mosca tse-tse Trypanosoma brucei Leishmaniasis Flebotomos hembras Parásitos Leishmania Esquistosomiasis Caracol de agua dulce Platelmintos (género Schistosoma) Fiebre del Nilo Occ. Mosquito Virus del Nilo Occidental Encefalitis japonesa Mosquito (género Culex) Virus de la encefalitis japonesa Fiebre amarilla Mosquito (géneros Aedes y Haemagogus) Virus de la fiebre amarilla
Malaria - Diagnóstico de vanguardia para la gestión y eliminación de la enfermedad
El diagnóstico rápido y preciso de las enfermedades nuevas y/o asintomáticas es fundamental para el tratamiento, control y eliminación efectivos de las enfermedades transmitidas por vectores. Dentro de las soluciones de diagnóstico disponibles actualmente se encuentran innovadoras pruebas de laboratorio que incluyen técnicas de amplificación de ácidos nucleicos (NAAT en inglés), pruebas de diagnóstico rápido (RDT en inglés) así como también análisis microscópico tradicional de muestras de sangre.
De las cinco especies de parásitos Plasmodium, 4 de ellas (P. falciparum, P. vivax, P. ovale, y P. malariae) causan la malaria humana. En los humanos los parásitos se multiplican exponencialmente en el hígado y después de varias etapas de desarrollo en los glóbulos rojos infectados.
Aunque las especies P. falciparum y P. vivax son las especies más importantes debido a su extendida prevalencia, la malaria causada por P. falciparum es la forma más letal2. El parásito falciparum puede eludir el sistema inmune la mayor parte de su ciclo de vida, se reproduce rápidamente en la sangre de tal manera que la infección puede progresar rápidamente hasta el punto de convertirse en grave. Además, P. falciparum hace que la características superficiales de los hematíes infectados cambien haciéndolos "pegajosos". Estos hematíes se adhieren a las células endoteliales que recubren el lumen de los vasos sanguíneos. La propiedad adhesiva de los hematíes genera el riesgo principal de oclusiones vasculares, especialmente en los capilares, causando malaria cerebral o renal que puede resultar en hipoxia y daño serio en órganos.
Productos relacionados
Datos y cifras de interés
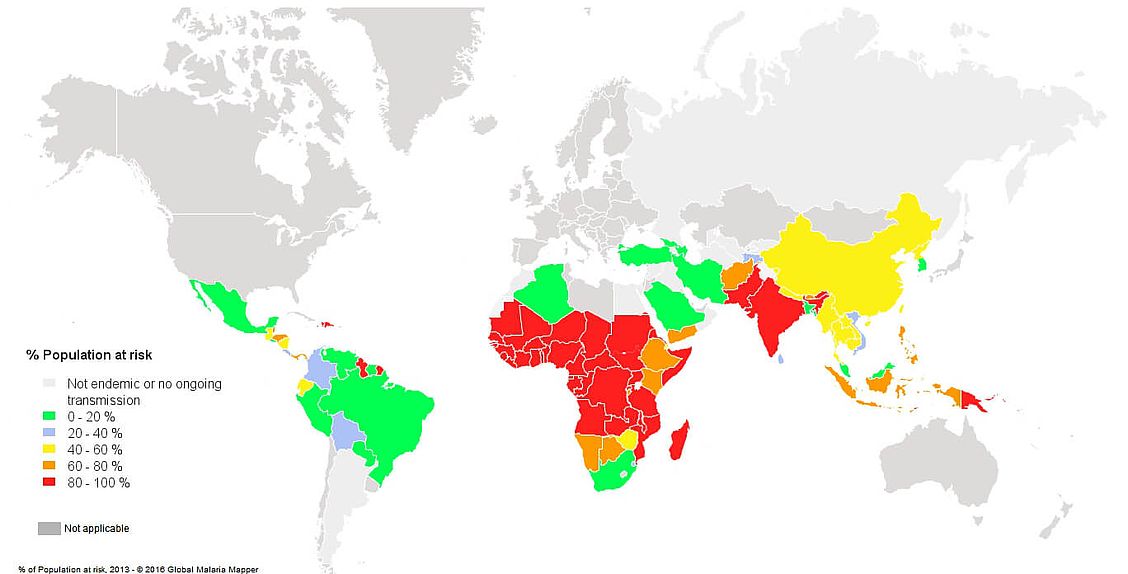
- Riesgo: Se estima que unas 3.4 mil millones de personas en el mundo se encuentran en riesgo (Fig. 1)
- Morbilidad y mortalidad: 207 millones de casos clínicos y 627.000 defunciones en 2012
- Mortalidad en 2010: 91% de las defunciones solo en África
Población en riesgo
Población en riesgo de contraer malaria según datos de 20133
Desafíos en el diagnóstico de la malaria
Un diagnóstico rápido y preciso es fundamental para el tratamiento, control y eliminación efectivos de la malaria. El tratamiento no selectivo contra la malaria para enfermedades sospechosas contribuye al aumento de los niveles de resistencia a fármacos antimaláricos (FIND). Actualmente la OMS recomienda la realización de un diagnóstico rápido en pacientes con sospecha de malaria por medio de pruebas microscópicas o pruebas de diagnóstico rápido (RDT).
La desventaja de la microscopía es que requiere de especialistas competentes bien entrenados, lo que resulta poco práctico en áreas con limitaciones. Es por ello que las pruebas diagnósticas rápidas (RDT) son ideales en áreas que no cuentan con las comodidades de los laboratorios especializados. Sin embargo, solo unas pocas de las pruebas de diagnóstico rápidas disponibles pueden detectar directamente las infecciones por P. vivax y ninguna puede detectar los reservorios latentes del parásito vivax en el hígado, vea debajo.
Además las infecciones subclínicas en áreas remotas no pueden diagnosticarse.
Sensibles como la PCR y sólidas como las pruebas de diagnóstico rápidas
Las técnicas de amplificación de ácidos nucleicos (NAAT) como la PCR en tiempo real son capaces de detectar infecciones subclínicas microscópicas. Aún así, la PCR en tiempo real sigue siendo inaccesible en áreas remotas de recursos limitados debido a que requiere de una infraestructura costosa, reactivos y pericia técnica. Las técnicas de diagnóstico molecular isotérmicas como la amplificación isotérmica mediada por bucle (LAMP), la amplificación isotérmica de ácidos nucleicos basada en secuencia (NASBA), la amplificación termofílica dependiente de helicasa (tHDA) y la amplificación de la polimerasa recombinasa (RPA) tienen la ventaja de combinar alta sensibilidad analítica con requerimientos técnicos que facilitan su implementación incluso en áreas de difícil acceso. No obstante, de acuerdo a FIND, el método LAMP se ha convertido en un precursor en este respecto ya que ofrece los beneficios de un análisis sensible y específico en combinación con requisitos mínimos de implementación así como también alta capacidad de rendimiento4,5. De esta manera, el método LAMP abre la puerta para campañas y proyectos efectivos en la eliminación de la malaria. En el futuro cercano será posible la detección específica de malaria vivax por medio de LAMP.
En resumen, el control y eliminación de la malaria requiere de una detección fiable de los casos subclínicos. La buena noticia es que sí existen tecnologías apropiadas a disposición.
Consideraciones importantes en el diagnóstico de malaria
- Recaídas de la malaria
P. vivax cuenta con una capacidad única en su ciclo de vida, ya que tras invadir los hepatocitos humanos puede seguir con su curso de infección o permanecer durante un periodo largo de tiempo en forma de hipnozoitos latentes. Luego de una activación subsiguiente que puede ocurrir después de algunos meses o incluso varios años, los hipnozoitos causan síntomas clínicos en ausencia de una nueva picadura del mosquito2. Los hipnozoitos son difíciles de detectar puesto que el parásito se envuelve en la membrana celular de la célula hepática huésped donde se encuentra relativamente protegido de ataques del sistema inmunitario del paciente6. Actualmente existe carencia de marcadores biológicos y técnicas de diagnóstico que puedan detectar los hipnozoitos latentes. La única forma de diagnosticar los pacientes con el estadio hepático latente es después de la activación de los hipnozoitos y la recaída subsiguiente. - Resistencia al P. vivax en algunas poblaciones
La distribución del P. vivax es más amplia que la del P. falciparum porque puede desarrollarse en el mosquito Anopheles a temperaturas bajas y puede sobrevivir en altas altitudes y en climas templados. Además puede formar hipnozoitos latentes. P. vivax utiliza el antígeno Duffy, presente en eritrocitos como receptores para fijarlos e invadirlos. Por lo tanto, los individuos con eritrocitos que presentan insuficiencia del antígeno Duffy, como es el caso de muchas poblaciones de África son resistentes a la infección7. Sin embargo, se han reportado casos de presencia del P. vivax en individuos con Duffy negativo, lo que sugiere que los receptores eritrocitarios aparte del antígeno Duffy pueden utilizarse para invadir los eritrocitos8. Tales hallazgos revelan el enorme impacto que esto podría tener en la distribución del P. vivax y se deben considerar en el diagnóstico de la malaria. - Resistencia a fármacos contra la malaria
La emergencia de la resistencia a fármacos contra el P. falciparum de la malaria es alarmante en países de Asia y África, lo cual representa una amenaza a los avances en la reducción de la morbilidad y mortalidad de la malaria9. Antes de iniciar el tratamiento se debe considerar realizar pruebas de diagnóstico de resistencia a fármacos contra la malaria.
Referencias
- World Health Day 2014 campaign. (accessed on 01.08.2014).
- World Health Organization Web site, WHO Global Malaria Programme: World Malaria Report: 2013.
- Global Malaria Mapper. (accessed on 18.10.2016).
- Vallejo, A.F., et al., Evaluation of the loop mediated isothermal DNA amplification (LAMP) kit for malaria diagnosis in P. vivax endemic settings of Colombia. PLoS Negl Trop Dis, 2015. 9.
- Hopkins, H., et al., Highly sensitive detection of malaria parasitemia in a malaria-endemic setting: performance of a new loop-mediated isothermal amplification kit in a remote clinic in Uganda. J Infect Dis, 2013. 208.
- Vaughan, A.M., A.S.I. Aly, and S.H.I. Kappe, Malaria Parasite Pre-Erythrocytic Stage Infection: Gliding and Hiding. Cell Host & Microbe. 4(3): p. 209-218.
- Zimmerman, P.A., et al., Red blood cell polymorphism and susceptibility to Plasmodium vivax. Adv Parasitol, 2013. 81: p. 27-76.
- Mendes, C., et al., Duffy negative antigen is no longer a barrier to Plasmodium vivax--molecular evidences from the African West Coast (Angola and Equatorial Guinea). PLoS Negl Trop Dis, 2011. 5(6): p. e1192.
- Ashley, E.A., et al., Spread of Artemisinin Resistance in Plasmodium falciparum Malaria. N Engl J Med, 2014. 371(5): p. 411-423.
- Britton, S., Q. Cheng, and J.S. McCarthy, Novel molecular diagnostic tools for malaria elimination: a review of options from the point of view of high-throughput and applicability in resource limited settings. Malar J, 2016. 15: p. 88.